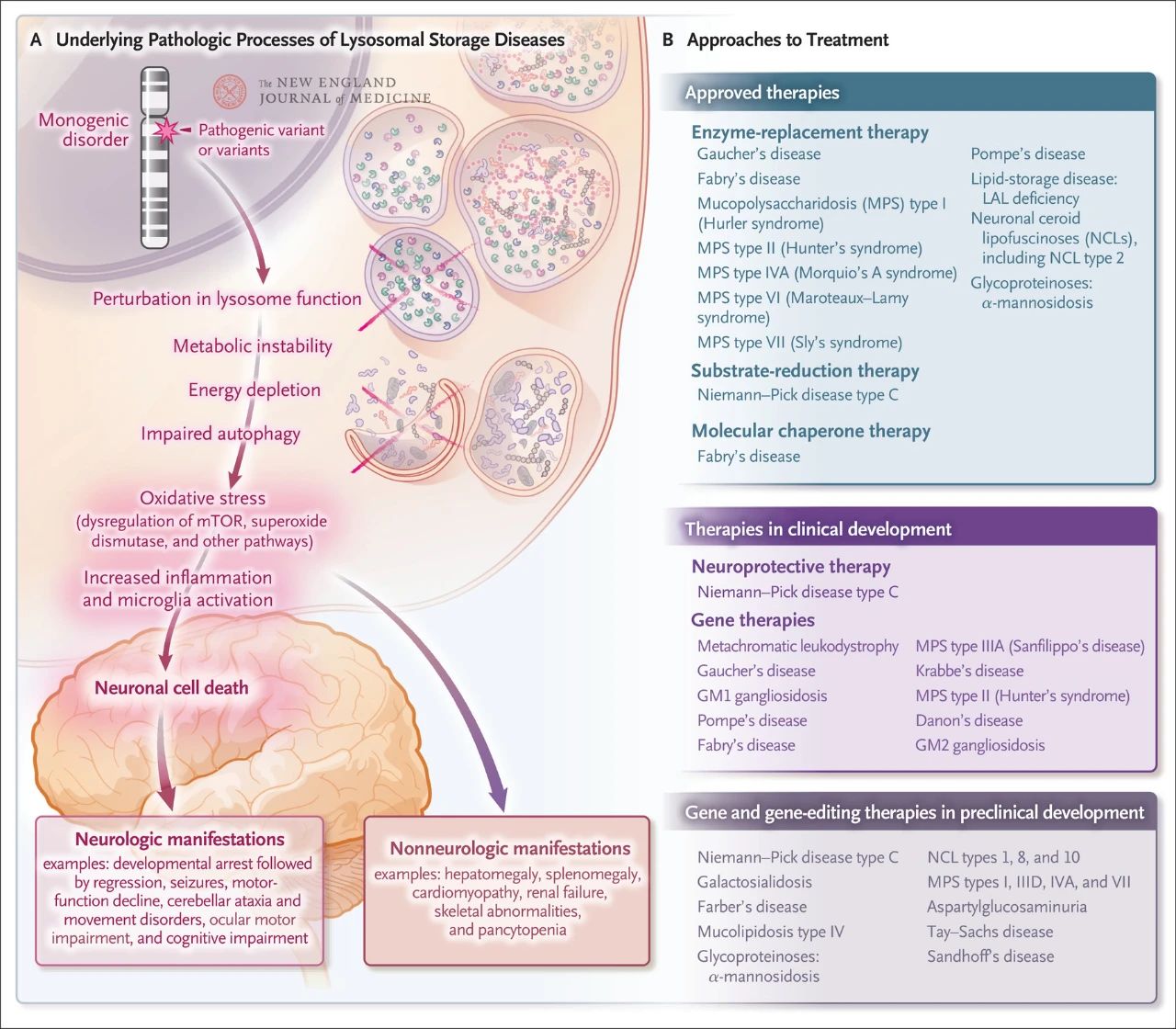
Iako relativno rijetka, ukupna incidencija lizozomskog skladištenja je oko 1 na svakih 5.000 živorođene djece. Osim toga, od skoro 70 poznatih poremećaja lizozomskog skladištenja, 70% pogađa centralni nervni sistem. Ovi poremećaji jednog gena uzrokuju lizozomsku disfunkciju, što rezultira metaboličkom nestabilnošću, disregulacijom ciljnog proteina rapamicina kod sisara (mTOR, koji normalno inhibira upalu), oštećenom autofagijom i smrću nervnih ćelija. Nekoliko terapija usmjerenih na osnovne patološke mehanizme lizozomske bolesti skladištenja je odobreno ili je u razvoju, uključujući terapiju zamjene enzima, terapiju redukcijom supstrata, terapiju molekularnim šaperonima, gensku terapiju, uređivanje gena i neuroprotektivnu terapiju.
Niemann-Pickova bolest tipa C je poremećaj ćelijskog transporta holesterola u lizozomima uzrokovan bialelnim mutacijama u NPC1 (95%) ili NPC2 (5%). Simptomi Niemann-Pickove bolesti tipa C uključuju brzo, fatalno neurološko propadanje u djetinjstvu, dok kasni juvenilni, juvenilni i odrasli oblici uključuju splenomegaliju, supranuklearnu paralizu pogleda i cerebelarnu ataksiju, dizartikulaciju i progresivnu demenciju.
U ovom izdanju časopisa, Bremova-Ertl i saradnici izvještavaju o rezultatima dvostruko slijepog, placebom kontroliranog, unakrsnog ispitivanja. U ispitivanju je korišten potencijalni neuroprotektivni agens, analog aminokiseline N-acetil-L-leucin (NALL), za liječenje Niemann-Pickove bolesti tipa C. Regrutirano je 60 simptomatskih adolescentnih i odraslih pacijenata, a rezultati su pokazali značajno poboljšanje ukupnog rezultata (primarni cilj) na Skali procjene i ocjenjivanja ataksije.
Klinička ispitivanja N-acetil-DL-leucina (Tanganil), racemika NALL-a i n-acetil-D-leucina, čini se da su uglavnom vođena iskustvom: mehanizam djelovanja nije jasno razjašnjen. N-acetil-DL-leucin je odobren za liječenje akutnog vertiga od 1950-ih; Životinjski modeli sugeriraju da lijek djeluje tako što rebalansira prekomjernu polarizaciju i depolarizaciju medijalnih vestibularnih neurona. Nakon toga, Strupp i saradnici su izvijestili o rezultatima kratkoročne studije u kojoj su uočili poboljšanja simptoma kod 13 pacijenata s degenerativnom cerebelarnom ataksijom različitih etiologija, nalazi koji su ponovo probudili interes za ponovno proučavanje lijeka.
Mehanizam kojim n-acetil-DL-leucin poboljšava funkciju živaca još nije jasan, ali nalazi na dva modela miševa, jednom s Niemann-Pickovom bolešću tipa C i drugom s poremećajem skladištenja gangliozida GM2 varijante O (Sandhoffova bolest), još jednom neurodegenerativnom lizozomskom bolešću, potaknuli su pažnju na NALL. Konkretno, preživljavanje Npc1-/- miševa tretiranih n-acetil-DL-leucinom ili NALL-om (L-enantiomeri) se poboljšalo, dok preživljavanje miševa tretiranih n-acetil-D-leucinom (D-enantiomeri) nije, što sugerira da je NALL aktivni oblik lijeka. U sličnoj studiji poremećaja skladištenja gangliozida GM2 varijante O (Hexb-/-), n-acetil-DL-leucin je rezultirao skromnim, ali značajnim produženjem životnog vijeka miševa.
Kako bi istražili mehanizam djelovanja n-acetil-DL-leucina, istraživači su istraživali metabolički put leucina mjerenjem metabolita u tkivima malog mozga mutiranih životinja. U varijantnom O modelu poremećaja skladištenja gangliozida GM2, n-acetil-DL-leucin normalizuje metabolizam glukoze i glutamata, povećava autofagiju i povećava nivoe superoksid dismutaze (aktivnog hvatača kiseonika). U C modelu Niemann-Pickove bolesti uočene su promjene u metabolizmu glukoze i antioksidansa te poboljšanja u metabolizmu mitohondrijalne energije. Iako je L-leucin snažan aktivator mTOR-a, nije bilo promjene u nivou ili fosforilaciji mTOR-a nakon tretmana n-acetil-DL-leucinom ili njegovim enantiomerima ni u jednom mišjem modelu.
Neuroprotektivni učinak NALL-a uočen je na mišjem modelu ozljede mozga izazvane kortikalnim impingementom. Ovi učinci uključuju snižavanje neuroinflamatornih markera, smanjenje smrti kortikalnih ćelija i poboljšanje fluksa autofagije. Nakon tretmana NALL-om, motoričke i kognitivne funkcije ozlijeđenih miševa su obnovljene, a veličina lezije je smanjena.
Upalni odgovor centralnog nervnog sistema je obilježje većine neurodegenerativnih poremećaja lizosomskog skladištenja. Ako se neuroinflamacija može smanjiti liječenjem NALL-om, klinički simptomi mnogih, ako ne i svih, neurodegenerativnih poremećaja lizosomskog skladištenja mogu se poboljšati. Kao što ova studija pokazuje, očekuje se da će NALL imati sinergiju s drugim terapijama za bolest lizosomskog skladištenja.
Mnogi poremećaji skladištenja lizosoma također su povezani s cerebelarnom ataksijom. Prema međunarodnoj studiji koja je uključivala djecu i odrasle s poremećajima skladištenja GM2 gangliozida (Tay-Sachsova bolest i Sandhoffova bolest), ataksija je smanjena, a koordinacija fine motorike poboljšana nakon liječenja NALL-om. Međutim, veliko, multicentrično, dvostruko slijepo, randomizirano, placebo kontrolirano ispitivanje pokazalo je da n-acetil-DL-leucin nije bio klinički učinkovit kod pacijenata s miješanom (nasljednom, nenasljednom i neobjašnjivom) cerebelarnom ataksijom. Ovo otkriće sugerira da se učinkovitost može primijetiti samo u ispitivanjima koja uključuju pacijente s nasljednom cerebelarnom ataksijom i analiziranim povezanim mehanizmima djelovanja. Osim toga, budući da NALL smanjuje neuroinflamaciju, koja može dovesti do traumatske ozljede mozga, mogu se razmotriti ispitivanja NALL-a za liječenje traumatske ozljede mozga.
Vrijeme objave: 02.03.2024.