Alzheimerova bolest, najčešći slučaj starijih osoba, muči većinu ljudi.
Jedan od izazova u liječenju Alzheimerove bolesti je taj što je dostava terapijskih lijekova u moždano tkivo ograničena krvno-moždanom barijerom. Studija je otkrila da fokusirani ultrazvuk niskog intenziteta vođen magnetnom rezonancom može reverzibilno otvoriti krvno-moždanu barijeru kod pacijenata s Alzheimerovom bolešću ili drugim neurološkim poremećajima, uključujući Parkinsonovu bolest, tumore mozga i amiotrofičnu lateralnu sklerozu.
Nedavno malo ispitivanje koncepta provedeno na Rockefeller institutu za neuroznanost na Univerzitetu Zapadne Virginije pokazalo je da pacijenti s Alzheimerovom bolešću koji su primili infuziju adukanumaba u kombinaciji s fokusiranim ultrazvukom privremeno otvaraju krvno-moždanu barijeru, što značajno smanjuje opterećenje beta-amiloida (Aβ) u mozgu na strani ispitivanja. Istraživanje bi moglo otvoriti nove mogućnosti liječenja poremećaja mozga.
Krvno-moždana barijera štiti mozak od štetnih supstanci, a istovremeno omogućava prolaz esencijalnih nutrijenata. Međutim, krvno-moždana barijera također sprječava dostavu terapijskih lijekova u mozak, što je posebno akutan izazov pri liječenju Alzheimerove bolesti. Kako svijet stari, broj ljudi s Alzheimerovom bolešću raste iz godine u godinu, a mogućnosti liječenja su ograničene, što predstavlja veliko opterećenje za zdravstvenu zaštitu. Aducanumab je monoklonsko antitijelo koje veže amiloid beta (Aβ) i koje je odobrila Američka agencija za hranu i lijekove (FDA) za liječenje Alzheimerove bolesti, ali je njegovo prodiranje kroz krvno-moždanu barijeru ograničeno.
Fokusirani ultrazvuk proizvodi mehaničke valove koji izazivaju oscilacije između kompresije i razrjeđivanja. Kada se ubrizgaju u krv i izlože ultrazvučnom polju, mjehurići se komprimiraju i šire više od okolnog tkiva i krvi. Ove oscilacije stvaraju mehanički stres na stijenku krvnog suda, uzrokujući istezanje i otvaranje čvrstih veza između endotelnih ćelija (slika ispod). Kao rezultat toga, integritet krvno-moždane barijere je ugrožen, što omogućava molekulima da difundiraju u mozak. Krvno-moždana barijera se sama zacjeljuje za oko šest sati.
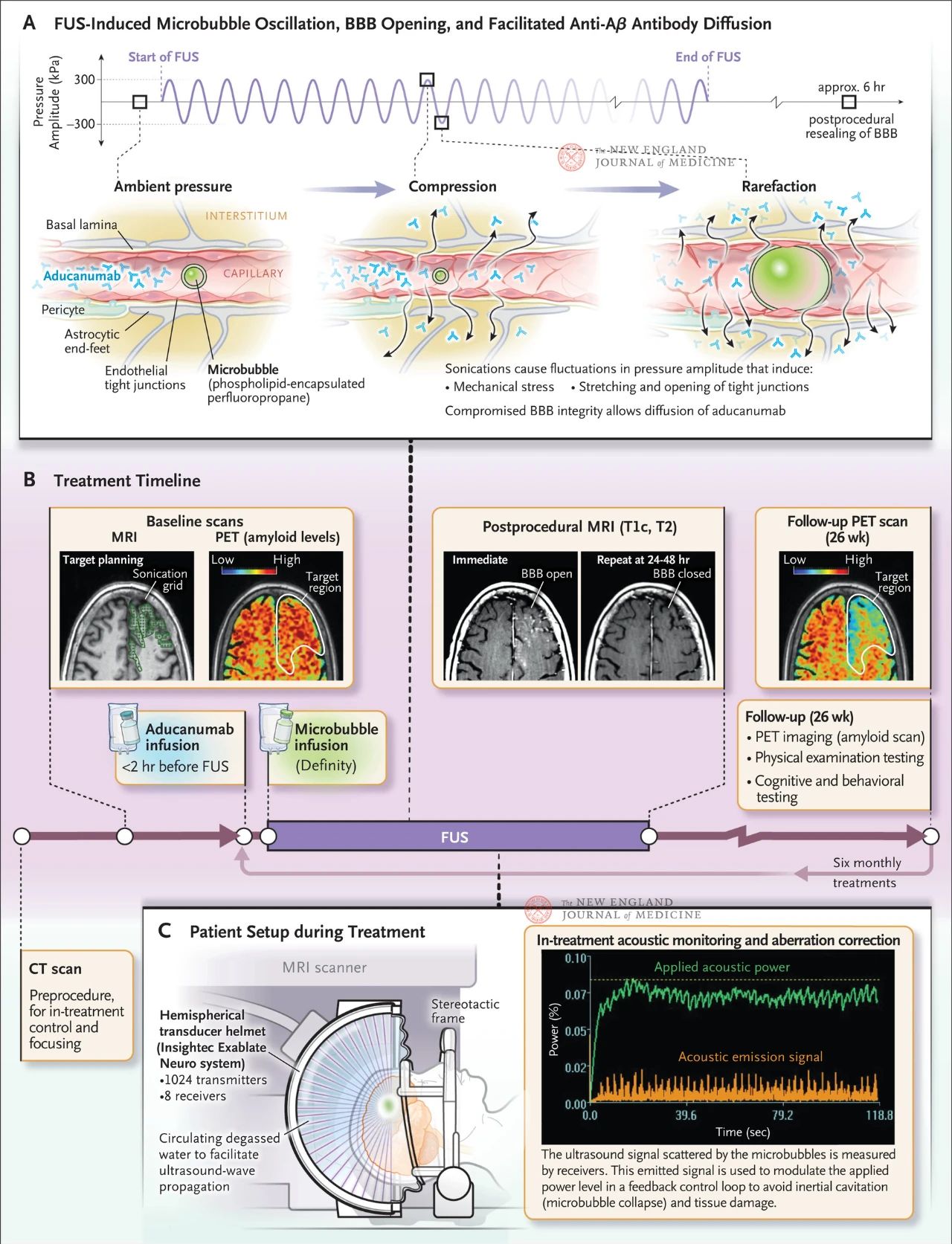
Slika prikazuje učinak usmjerenog ultrazvuka na zidove kapilara kada su u krvnim sudovima prisutni mjehurići mikrometarske veličine. Zbog visoke kompresibilnosti plina, mjehurići se skupljaju i šire više od okolnog tkiva, uzrokujući mehanički stres na endotelne ćelije. Ovaj proces uzrokuje otvaranje čvrstih veza i može uzrokovati i otpadanje završetaka astrocita sa zida krvnog suda, ugrožavajući integritet krvno-moždane barijere i potičući difuziju antitijela. Osim toga, endotelne ćelije izložene fokusiranom ultrazvuku pojačale su svoju aktivnu aktivnost vakuolarnog transporta i potisnule funkciju efluksne pumpe, čime su smanjile uklanjanje antitijela iz mozga. Slika B prikazuje raspored liječenja, koji uključuje kompjuteriziranu tomografiju (CT) i magnetnu rezonancu (MRI) za razvoj plana ultrazvučnog liječenja, pozitronsku emisionu tomografiju (PET) 18F-flubitabana na početku, infuziju antitijela prije fokusiranog ultrazvučnog tretmana i mikrovezikularnu infuziju tokom tretmana, te akustično praćenje ultrazvučnih signala mikrovezikularnog raspršenja koji se koriste za kontrolu tretmana. Slike dobivene nakon fokusiranog ultrazvučnog tretmana uključivale su T1-ponderiranu MRI s kontrastom, koja je pokazala da je krvno-moždana barijera otvorena u području tretiranom ultrazvukom. Slike istog područja nakon 24 do 48 sati fokusiranog ultrazvučnog tretmana pokazale su potpuno zacjeljivanje krvno-moždane barijere. PET skeniranje sa 18F-flubitabanom tokom praćenja kod jednog od pacijenata 26 sedmica kasnije pokazalo je smanjene nivoe Aβ u mozgu nakon tretmana. Slika C prikazuje MRI-vođenu fokusiranu ultrazvučnu postavku tokom tretmana. Hemisferična kaciga sa transduktorom sadrži više od 1.000 ultrazvučnih izvora koji konvergiraju u jednu fokalnu tačku u mozgu koristeći MRI vođenje u realnom vremenu.
U studijama na životinjama 2001. godine prvi put je pokazano da fokusirani ultrazvuk izaziva otvaranje krvno-moždane barijere, a naknadne predkliničke studije su pokazale da fokusirani ultrazvuk može poboljšati isporuku i efikasnost lijekova. Od tada je utvrđeno da fokusirani ultrazvuk može sigurno otvoriti krvno-moždanu barijeru kod pacijenata s Alzheimerovom bolešću koji ne primaju lijekove, a također može isporučiti antitijela na metastaze raka dojke u mozgu.
Proces isporuke mikromjehurića
Mikromjehurići su ultrazvučno kontrastno sredstvo koje se obično koristi za posmatranje protoka krvi i krvnih sudova u ultrazvučnoj dijagnostici. Tokom ultrazvučne terapije, intravenski je ubrizgana suspenzija oktafluoropropana u obliku nepirogenih mjehurića obloženih fosfolipidima (Slika 1B). Mikromjehurići su visoko polidispergirani, s promjerima u rasponu od manje od 1 μm do više od 10 μm. Oktafluoropropan je stabilan plin koji se ne metabolizira i može se izlučivati putem pluća. Lipidna ovojnica koja obavija i stabilizira mjehuriće sastoji se od tri prirodna ljudska lipida koji se metaboliziraju na sličan način kao i endogeni fosfolipidi.
Generisanje fokusiranog ultrazvuka
Fokusirani ultrazvuk generira se pomoću hemisferične kacige s pretvaračem koja okružuje glavu pacijenta (Slika 1C). Kaciga je opremljena s 1024 nezavisno kontrolirana ultrazvučna izvora, koji su prirodno fokusirani u središtu hemisfere. Ovi ultrazvučni izvori pokreću se sinusoidnim radiofrekventnim naponima i emitiraju ultrazvučne valove vođene magnetskom rezonancijom. Pacijent nosi kacigu, a degazirana voda cirkulira oko glave kako bi se olakšao prijenos ultrazvuka. Ultrazvuk putuje kroz kožu i lubanju do ciljanog mozga.
Promjene u debljini i gustoći lubanje utjecat će na širenje ultrazvuka, što rezultira neznatno različitim vremenom potrebnim da ultrazvuk stigne do lezije. Ovo izobličenje se može ispraviti prikupljanjem podataka kompjuterizirane tomografije visoke rezolucije kako bi se dobile informacije o obliku, debljini i gustoći lubanje. Model kompjuterske simulacije može izračunati kompenzirani fazni pomak svakog pogonskog signala kako bi se vratio oštar fokus. Kontroliranjem faze RF signala, ultrazvuk se može elektronički fokusirati i pozicionirati tako da pokrije velike količine tkiva bez pomicanja niza ultrazvučnih izvora. Lokacija ciljnog tkiva određuje se magnetskom rezonancijom glave dok se nosi kaciga. Ciljani volumen je ispunjen trodimenzionalnom mrežom ultrazvučnih sidrišnih tačaka, koje emitiraju ultrazvučne valove na svakoj sidrišnoj tački tokom 5-10 ms, ponavljajući se svake 3 sekunde. Ultrazvučna snaga se postepeno povećava dok se ne detektira željeni signal raspršenja mjehurića, a zatim se drži 120 sekundi. Ovaj proces se ponavlja na drugim mrežama dok se ciljni volumen potpuno ne pokrije.
Otvaranje krvno-moždane barijere zahtijeva da amplituda zvučnih valova pređe određeni prag, nakon kojeg se permeabilnost barijere povećava s povećanjem amplitude pritiska sve dok ne dođe do oštećenja tkiva, što se manifestira kao egzosmoza eritrocita, krvarenje, apoptoza i nekroza, a sve to je često povezano s kolapsom mjehurića (nazvana inercijalna kavitacija). Prag ovisi o veličini mikromjehurića i materijalu ljuske. Detekcijom i interpretacijom ultrazvučnih signala raspršenih mikromjehurićima, izloženost se može održati u sigurnom rasponu.
Nakon ultrazvučnog tretmana, korištena je T1-ponderirana magnetna rezonanca s kontrastnim sredstvom kako bi se utvrdilo je li krvno-moždana barijera otvorena na ciljanoj lokaciji, a T2-ponderirane slike korištene su za potvrdu je li došlo do ekstravazacije ili krvarenja. Ova zapažanja pružaju smjernice za prilagođavanje drugih tretmana, ako je potrebno.
Evaluacija i izgledi za terapijski učinak
Istraživači su kvantificirali učinak tretmana na opterećenje mozga Aβ upoređujući 18F-flubitaban pozitronsku emisionu tomografiju prije i nakon tretmana kako bi procijenili razliku u volumenu Aβ između tretiranog područja i sličnog područja na suprotnoj strani. Prethodna istraživanja istog tima pokazala su da jednostavno fokusiranje ultrazvuka može neznatno smanjiti nivoe Aβ. Smanjenje uočeno u ovom ispitivanju bilo je čak i veće nego u prethodnim studijama.
U budućnosti, proširenje tretmana na obje strane mozga bit će ključno za procjenu njegove efikasnosti u odgađanju progresije bolesti. Osim toga, potrebna su daljnja istraživanja kako bi se utvrdila dugoročna sigurnost i efikasnost, a za širu dostupnost moraju se razviti isplativi terapijski uređaji koji se ne oslanjaju na online MRI smjernice. Ipak, nalazi su izazvali optimizam da bi tretman i lijekovi koji uklanjaju Aβ na kraju mogli usporiti progresiju Alzheimerove bolesti.
Vrijeme objave: 06.01.2024.